2025年8月5日,中国科学院微生物研究所邓涛团队在Journal of Virology在线发表了题为The 5’-end segment-specific noncoding region of influenza A virus regulates both competitive multi-segment RNA transcription and selective genome packaging during infection的研究论文。该研究深入解析了病毒基因组5’端片段特异性非编码区的双重功能:不仅介导基因组的选择性包装,还参与调控多模板竞争性病毒RNA的转录。
甲型流感病毒(IAV)基因组由8个RNA片段组成,其3’和5’端包含片段特异性或亚型特异性(在HA和NA片段中)的非编码区(ssNCRs),这些区域位于高度保守的末端启动子序列与编码起始或终止密码子之间,因长度和序列在不同IAV的同一片段上高度一致,长期被视作基因组选择性包装的关键信号。然而,对其在病毒RNA合成阶段的作用却知之甚少。前期,邓涛团队发现,3’端的H1-ssNCR及其相邻的编码区可在多模板环境中下调控H1 片段RNA(vRNA)的竞争性合成(Journal of Virology,2021)。
本研究通过对5’端H1-ssNCR进行系列截短发现,与3’端不同,截短5’H1-ssNCR会以模板竞争的方式导致HA mRNA水平下降(但不显著影响vRNA水平),并削弱HA vRNA在子代病毒中的包装。值得关注的是,携带严重截短的5’H1-ssNCR的重组病毒经传代在截短位点上游7个核苷酸处出现了一个可恢复病毒复制效率的适应性同义突变,解析该突变的作用机制发现它能恢复5’H1-ssNCR截短后的竞争性转录效率与包装效率;最后通过预测5’H1-ssNCR附近的RNA二级结构,推测回复突变可能逆转了5’H1-ssNCR截短造成的RNA结构自由能改变,提示5’-ssNCR附近的RNA二级结构可能参与调控竞争性转录和选择性包装。以上研究成果创新性地提出了IAV片段特异性非编码区在病毒多片段竞争性环境中发挥调控作用,为理解IAV基因组关键序列与结构特征在病毒复制和进化中的作用提供了新的理论基础,也为开发靶向病毒RNA的新型抗病毒药物奠定了重要的理论基础。
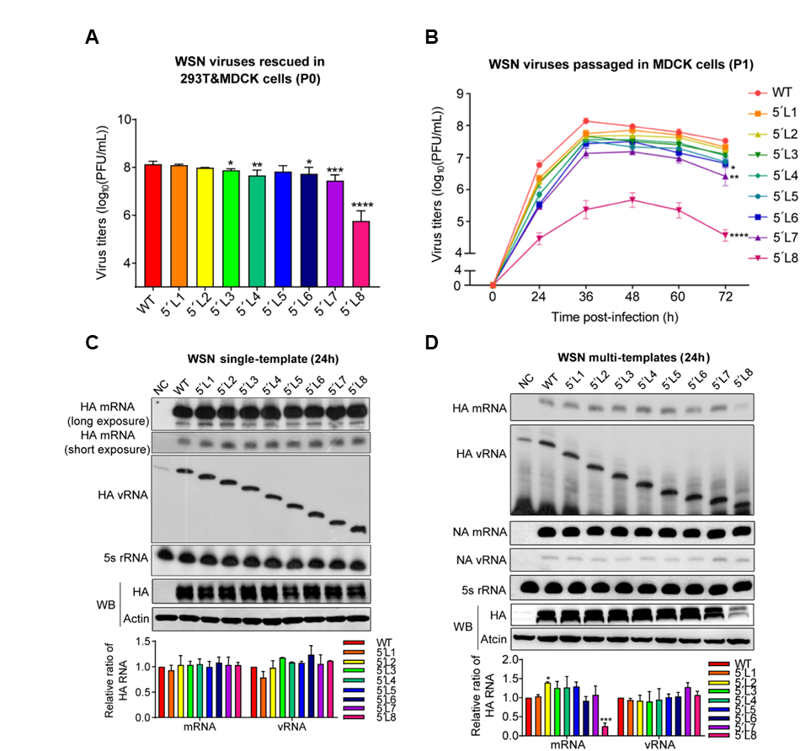
图1 HA 5’端片段特异性非编码区截短使病毒滴度下降并以模板竞争的方式降低HA mRNA水平
中国科学院微生物研究所博士研究生刘子宁为论文第一作者,微生物所邓涛研究员为本文通讯作者。
原文链接:https://doi.org/10.1128/jvi.00328-25




