
- 高级人才招聘
- 中、初级专业技术人才招聘
- 管理、支撑岗位招聘
- 博士后招聘
2024年,世界卫生组织将耐碳青霉烯类肺炎克雷伯菌列为优先级最高的病原体之一,凸显了应对该病原菌的全球紧迫性。噬菌体作为对抗耐药菌的重要武器,为抑制肺炎克雷伯菌提供了有效手段。然而,该菌表面荚膜抗原的高度异质性,导致天然噬菌体杀菌谱极为狭窄,难以直接应用于临床。如何拓宽噬菌体的靶向范围,成为工程化改造的核心目标,而这依赖于对噬菌体遗传信息的深度挖掘。 面对日益增长的噬菌体基因组数据,如何从海量序列中挖掘有效信息,将其转化为靶向精准、可编程设计的工程化噬菌体制剂,已成为突破当前应用瓶颈的关键。
近日,中国科学院微生物研究所冯婕团队在工程化噬菌体对抗耐药细菌领域取得重要进展。该研究以Przondovirus 属噬菌体为对象,揭示了噬菌体受体结合蛋白簇与肺炎克雷伯菌荚膜(KL)型之间的精确对应关系,同时提出一种创新的“表型工程化”策略,成功建立了一套从数据挖掘到工程化噬菌体构建的完整合成生物学框架。
团队通过大规模挖掘公共数据库,将Przondovirus 属噬菌体的受体结合蛋白序列划分为50余个独立簇。结合生化筛选实验对代表性蛋白进行验证,系统确证了受体结合蛋白簇与特定KL型间的靶向决定关系,同时将该属噬菌体所识别的KL型从已知的14个拓展至32个,并以此构建了标准化元件库。基于对噬菌体尾部组装机制的解析,团队利用受体结合蛋白保守结构域作为通用分子接口,开发出创新的表型工程化策略:通过在宿主内反式表达外源受体结合蛋白变体,使其能够“即插即用”地无缝整合至子代噬菌体颗粒中。该策略无需复杂的基因组编辑即可精准拓宽宿主范围,且子代基因组保持野生型不变,兼顾了临床应用的高效性与环境生态安全性。
该研究建立的数据驱动型合成生物学框架,将线上基因组数据转化为了模块化工具集,攻克了噬菌体宿主谱难以预测和精准调控的技术瓶颈,为应对多重耐药菌感染提供了精准、灵活的技术范式,为未来“按需定制”新型抗菌制剂奠定了科学基础。
微生物所博士研究生荆世松为论文第一作者,微生物所冯婕研究员和王超副研究员为论文的共同通讯作者。研究工作得到国家重点研发计划以及中国科学院国际伙伴计划项目等项目资助。
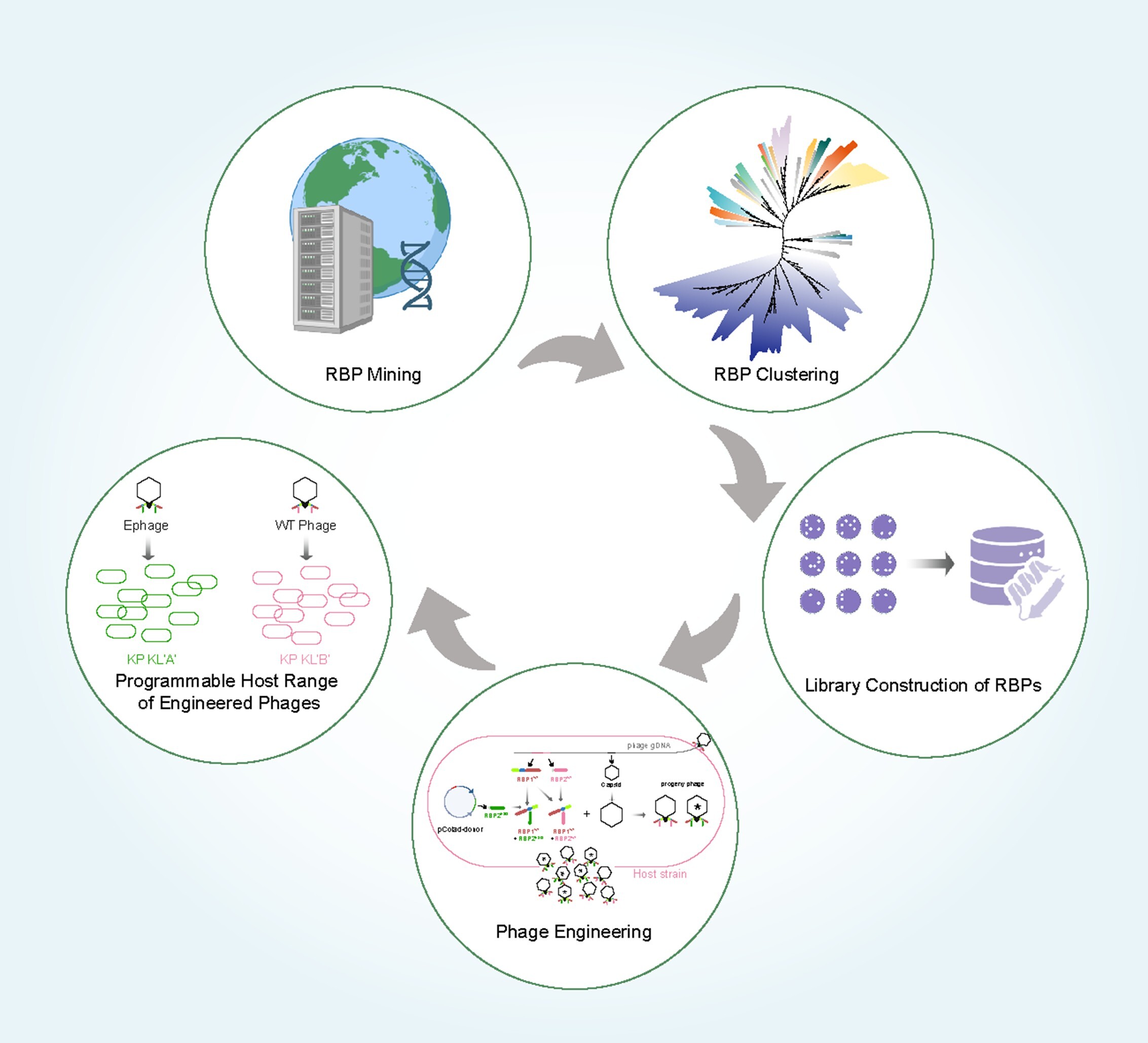
数据驱动的噬菌体受体结合蛋白挖掘及表型工程化流程示意图
文章链接:https://doi.org/10.1002/advs.202514511
附件下载: