
- 高级人才招聘
- 中、初级专业技术人才招聘
- 管理、支撑岗位招聘
- 博士后招聘
近日,中国科学院微生物研究所刘翠华团队、汪静团队与军事科学院军事医学研究院张令强团队合作,揭示了小GTPase Rab14作为广谱宿主限制因子,通过促进V-ATPase的溶酶体转运,进而介导溶酶体酸化及多种类病原体清除的重要机制。
刘翠华团队长期致力于结核病感染免疫机制研究,在探究结核分枝杆菌(Mtb)与宿主互作机制的过程中,发现多个与Mtb胞内存活密切相关的病原分泌性效应蛋白均共同靶向宿主的小GTPase Rab14,并揭示了Mtb劫持Rab14抑制宿主自噬流介导的病原清除机制(Autophagy,2022)。然而,Rab14在其它多种病原体感染免疫中的生理调控功能及作用机制尚未明确。
近期,团队进一步合作发现,在多种Mtb以外的细菌和病毒包括耻垢分枝杆菌、单核细胞增生李斯特菌以及单纯疱疹病毒和仙台病毒)感染条件下,Rab14可促进溶酶体酸化必需的关键复合物V-ATPase的转运,进而介导溶酶体酸化,最终实现对多种病原体的广谱清除。机制研究表明,不同于Mtb,上述病原体感染可诱导GTP结合形式的Rab14水平升高,并增强Rab14与钙调蛋白依赖性激酶CAMK2D之间的结合,进而抑制CAMK2D介导的V-ATPase关键亚基V0a1的磷酸化修饰;该抑制作用促使V0a1与COPII复合物结合,驱动V-ATPase经由内质网-高尔基体-溶酶体途径转运,最终增强溶酶体酸化能力并促进病原体清除。综上,该研究揭示了由Rab14-CAMK2D-V-ATPase轴介导的全新抗感染免疫通路,为多种细菌和病毒感染性疾病的精准宿主导向治疗提供了新靶点和新策略。该发现有望增强宿主主动免疫应答,降低病原体耐药的发生。
微生物所博士研究生雷泽慧和军事科学院军事医学研究院强丽华助理研究员为论文共同第一作者,微生物所刘翠华研究员、汪静研究员和军事科学院军事医学研究院张令强研究员为论文的共同通讯作者。研究工作得到国家自然科学基金、国家重点研发计划等项目资助。
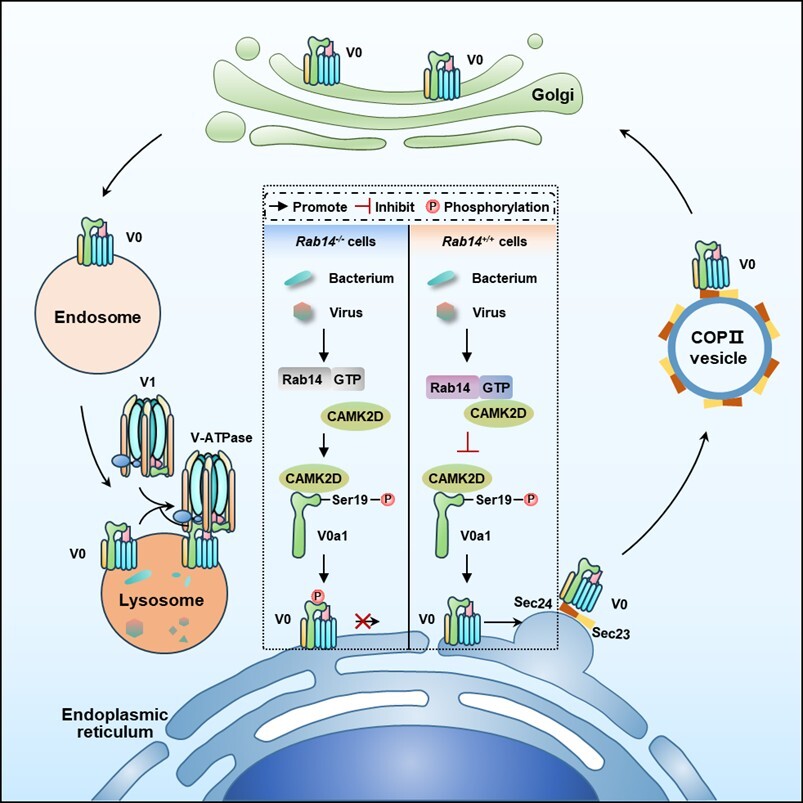
宿主Rab14促进V-ATPase的溶酶体转运进而介导
溶酶体酸化及病原体清除的机制示意图
文章链接: https://www.nature.com/articles/s41467-026-70258-w
附件下载: